morfoloģija
Makroskopiskā līmenī Alzheimera slimībā var novērot dažāda līmeņa kortikālo atrofiju (audu vai orgānu masas samazināšanos), ko raksturo parietālās vagas paplašināšanās, vairāk akcentēta frontālās, laikmetīgās un parietālās lobās. Šo atrofiju kompensē kambara dobumu palielināšanās, kas ir sekundāra parenchima zudumam (1. attēls). Jo īpaši slimības progresīvajos posmos mediālās īslaicīgās daivas struktūras, ieskaitot hippokampu, entorālo garozu un amygdalu, atrofija stipri, ņemot vērā to iesaisti no patoloģijas sākuma stadijām.
Turklāt Alcheimera slimība rada arī mikroskopiskas izmaiņas, kas pazīstamas kā ekstracelulārās senilās plāksnes un intracelulārās neirofibrilārās kopas, kas veido histoloģiskās diagnozes pamatu. Līdz ar slimības progresēšanu ir nopietns neironu zudums, ko papildina glioze (neirogliju šūnu ierobežota vai difūza izplatīšanās, reaktīva dabā, tas ir, šūnas, kas veido nervu audu atbalstošo stromu) tajos pašos reģionos. kur nefibrilāras plāksnes un klasteru klātbūtne ir lielāka.
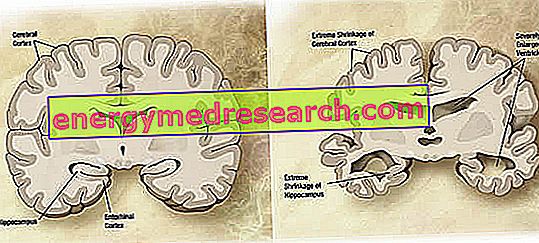
1. attēls . Smadzeņu koronālā daļa: atšķirības starp normālām smadzenēm un smadzenēm, ko ietekmē AD (wikipedia image source).
patoģenēzes
Alcheimera slimību raksturo galvenokārt divi tipiski bojājumi: senilu plākšņu ekstracelulārā uzkrāšanās, kas galvenokārt sastāv no β-amiloida peptīda (Aβ) un intranurālā neirofibrilārā klastera, ko veido hiperfosforilēts tau proteīns.
- Senilās plāksnes var atrast tādās smadzeņu teritorijās kā hipokamps, amigdala un neocortex.
Aβ peptīds rodas no amiloidu proteīnu prekursora (APP) proteolītiskās sagriešanas ar β-sekrēzi. Šis griezums ģenerē terminālo karboksīda fragmentu no 99 atlikumiem (CTF vai C99), ko pēc tam sagriež β-sekrēze, lai radītu Aβ fragmentus ar atšķirīgiem garumiem. Ir zināms, ka visbiežāk iegūtās Aβ sugas ir Aβ40 fragments. Vēl viens zināms fragments, kas veidojas no proteolītiskā griezuma, kas ir mazāks par Aβ40, ir Aβ42, kas ir vairāk pakļauts amiloidu fibriliem, kas uzkrājas kā Aβ sugas indivīda smadzenēs ar Alcheimera slimību.
- Citu sastāvdaļu, kas atrodas Alcheimera slimībā, pārstāv neirofibrilārie klasteri, kas sastāv no kvēldiega kostīmiem, kas atrodas neironu citoplazmā. Neirofibrillāras kopas ir nešķīstošas un, šķiet, ir izturīgas pret proteolīzes procesiem in vivo, tādējādi saglabājot audu sekcijās pat ilgu laiku pēc neironu nāves. Ievērojot struktūru, fibrillāros klasterus veido dubultā spirāles pavedieni un lineāras pavedieni ar līdzīgu sastāvu. Analizējot kompozīciju, divkāršās spirāles šķiedras lielākoties ir izgatavotas no hiperfosforilētā tau proteīna. Tau ir asins šūnu proteīns, kas saistīts ar mikrotubulām, kas atvieglo tā montāžu.
Citas svarīgas neiropatoloģiskas pārmaiņas Alcheimera slimībā ir mitohondriju disfunkcija, oksidatīvs neironu bojājums, sinaptisks zudums un axona deģenerācija.
Neiroķīmiskie aspekti
Kā jau minēts, Aβ peptīds, kas izriet no APP prekursora proteolītiskās griezuma, ir Alzheimera slimības neirotoksiska sastāvdaļa . Konkrētāk, ir pieņemts, ka Aβ var būt svarīga normālām smadzeņu funkcijām, un, ja tā pārvarēs noteiktas koncentrācijas, tā var kļūt neirotoksiska. Turklāt gan agregātiem, gan Aβ dažādajām izoformām varētu būt atšķirīga bioloģiskā, fizioloģiskā vai patoloģiskā loma, nosakot un piedaloties turpmākajos slimības posmos. Ir novērots, ka Aβ darbojas kā neiromodulators, kas ietekmē dažu neirotransmiteru izdalīšanos, ja nav acīmredzamu neirotoksicitātes pazīmju.
Piemēram, Aβ neiromodulējošajai lomai fizioloģiskā kontekstā var būt nozīmīga nozīme, lai pareizā līdzsvarā būtu neirotransmitera sistēma. Ir labi zināms, ka šī sistēma sastāv no neirotransmiteriem, vielām, kas sniedz informāciju starp šūnām, kas veido nervu sistēmu, neironus, izmantojot sinaptisko transmisiju.
Patoloģiskos apstākļos, no otras puses, A-mediētā sinaptiskā transmisija varētu būt saistīta ar neirotransmisijas maiņu pirms neirodeģeneratīviem notikumiem. Šo izmaiņu rezultātā var rasties agrīnie kognitīvie un ne-kognitīvie traucējumi, pamatojoties uz neirotransmiteru sistēmām un dažādām iesaistītajām smadzeņu zonām.
Ļoti sarežģītas ir neiromediatoru sistēmu pārmaiņas un signālu transdukcijas mehānisms indivīdu smadzenēs, kas cieš no Alcheimera slimības. Viena no sistēmām, kas, šķiet, ir mainījusies, attiecas uz holīnerģisko signalizācijas sistēmu, kas ietver neirotransmitera acetilholīnu. Patiešām, ir pierādīts, ka indivīdiem, kas slimo ar Alcheimera slimību, vērojama pazemināta holīnerģiskā transmisija garozas un hipokampusa līmenī, svarīgas smadzeņu zonas, kas veltītas tādām parādībām kā mācīšanās un atmiņa. Papildus šai neirotransmitera sistēmai Alzheimera slimībā ir novērotas noradrenerģiskās, serotonergiskās, kā arī glutamāta un GABA sistēmas izmaiņas.