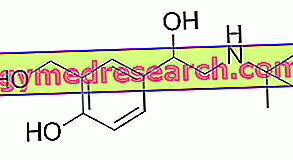
Kas ir Stayveer - Bosentan lieto un kādam nolūkam to lieto?
Stayveer ir zāles, kas satur aktīvo vielu bosentānu . Tas ir indicēts III klases pacientu ar plaušu arteriālo hipertensiju (PAH) ārstēšanai, lai uzlabotu fizisko slodzi un simptomus. PAH ir patoloģisks stāvoklis, kurā spiediens plaušu artērijās ir augsts. "Klase" norāda uz slimības smagumu: "III klase" ietver spēcīgu fiziskās aktivitātes ierobežošanu. PAO var būt:
- primārais (bez identificēta vai ģimenes cēloņa);
- ko izraisa sklerodermija (vai progresējoša sistēmiska skleroze, stāvoklis, ko raksturo ādas un citu orgānu atbalstoša saistaudu neparasta augšana);
- radušies iedzimtu sirds defektu dēļ (klāt no dzimšanas) ar šuntiem (elpceļu anomālijām), kas izraisa patoloģisku asins plūsmu starp sirdi un plaušām.
- Ir novēroti uzlabojumi arī pacientiem ar PAH II klasi. "II klase" ietver nelielu fiziskās aktivitātes ierobežojumu. Stayveer var lietot arī pieaugušajiem ar progresējošu sistēmisku sklerozi, kurā slikta asinsrite, ko izraisa slimība, ir izraisījusi "digitālo čūlu" parādīšanos (pirkstu un pirkstu iekaisums). Stayveer mērķis ir samazināt jaunu digitālo čūlu skaitu.
Šīs zāles ir tādas pašas kā Tracleer, kas jau ir reģistrētas Eiropas Savienībā (ES). Uzņēmums, kas ražo Tracleer, ir piekritis, ka tās zinātniskos datus var izmantot Stayveer ("informēta piekrišana").
Kā lieto Stayveer - Bosentan?
Stayveer var iegādāties tikai ar recepti un ārstēšanu jāsāk un jāuzrauga ārstam, kam ir pieredze PAH vai progresējošas sistēmiskas sklerozes ārstēšanā. Stayveer ir pieejams tabletēs (62, 5 mg un 125 mg), kas jānorij, uzdzerot ūdeni. Tabletes jālieto no rīta un vakarā. Pieaugušajiem sākumdeva ir 62, 5 mg divas reizes dienā četras nedēļas, pēc tam palielināta līdz parastajai 125 mg devai divas reizes dienā. Bērniem ar PAH lietojamā deva jāaprēķina, pamatojoties uz ķermeņa masu, un parasti tā sākas ar 2 mg uz kilogramu divas reizes dienā. Plašāku informāciju skatiet lietošanas instrukcijā. Ārsts novērtēs pacienta atbildes reakciju uz Stayveer un noteiks nepieciešamību turpināt ārstēšanu pēc astoņām nedēļām pacientiem ar PAH, kuriem nav ziņots par uzlabojumiem, kā arī regulāri pacientiem ar progresējošu sistēmisku sklerozi ar pašreizējām digitālām čūlām. Ja ārsts nolemj pārtraukt ārstēšanu ar Stayveer, deva pakāpeniski jāsamazina. Pacientiem, kuri tiek ārstēti ar Stayveer, jāsaņem īpašs memorands, kurā apkopota galvenā informācija par zāļu drošumu.
Kā Stayveer - Bosentan darbojas?
Stayveer aktīvā viela bosentāns inhibē dabā sastopamo hormonu endotelīnu-1 (ET-1), kas izraisa asinsvadu sašaurināšanos. Tāpēc Stayveer nosaka asinsvadu paplašināšanos. PAH ir novājinoša slimība, kurā notiek plaša asinsvadu sašaurināšanās plaušās. Tas izraisa ļoti augstu asinsspiedienu asinsvados, kas ved asinis no sirds labās puses uz plaušām. Šis spiediens samazina skābekļa daudzumu, ko asinis var pārvietot plaušās, padarot fizisko aktivitāti grūtāku. Paplašinot šos asinsvadus, samazinās asinsspiediens un uzlabojas simptomi. Pacientiem ar progresējošu sistēmisku sklerozi un notiekošām digitālām čūlas, bosentāns uzlabo asinsriti pirkstos un pirkstos, novēršot jaunu digitālo čūlu veidošanos.
Kāds ir Stayveer - Bosentan iedarbīgums šajos pētījumos?
PAH gadījumā Stayveer tika pētīts četros pamatpētījumos: divos pētījumos, kuros kopumā piedalījās 245 pieaugušie ar III vai IV klases PAH, kas bija primāri vai sklerodermiju izraisījuši, pētījums, kurā piedalījās 54 pieaugušie ar PAH III klasē. iedzimtiem sirds defektiem, kā arī pētījums ar 185 pacientiem ar PAH II klasē. Pētījumos tika salīdzināts Stayveer un placebo (viela, kas neietekmē ķermeni), abi tika pievienoti standarta terapijai. Galvenais efektivitātes rādītājs bija attālums, ko pacienti varēja staigāt sešās minūtēs (veids, kā izmērīt fizisko slodzi); tomēr pētījums par II klases slimību pārbaudīja arī asins plūsmas rezistences izmaiņas plaušu asinsvados (indikators, kas liecina par asinsvadu sašaurināšanos). PAH III vai IV klasei, kas bija primāra vai izraisījusi sklerodermija, abi pētījumi atklāja, ka pacienti, kas ārstēti ar Stayveer, pēc 16 ārstēšanas nedēļām (44 metri vairāk pētījumā) varēja segt garākus attālumus nekā pacienti, kas ārstēti ar placebo lielāks); tomēr pacientu skaits ar PAH IV klasē bija pārāk mazs, lai atbalstītu šīs zāles lietošanu šajā grupā. Līdzīgi rezultāti parādījās arī pacientiem ar iedzimtiem sirds defektiem. Pacientiem ar II klases PAH Stayveer izraisīja asinsvadu rezistences samazināšanos par 23%, salīdzinot ar placebo, pēc sešiem ārstēšanas mēnešiem, bet attālums, ko pacienti varēja staigāt sešās minūtēs, abās grupās bija līdzīgs. Tika veikts arī pētījums par 19 bērniem un pusaudžiem vecumā no 3 līdz 15 gadiem, kuros tika novēroti ar sirdi un artērijām saistītie parametri. Progresīvas sistēmiskas sklerozes gadījumā ar digitālajām čūlām, divos pētījumos Stayveer salīdzināja ar placebo kopumā 312 pieaugušajiem. Galvenais efektivitātes rādītājs balstījās uz jauno digitālo čūlu skaitu, kas radušās pētījumos. Vienā no pētījumiem tika pētīta arī Stayveer ietekme uz 190 pacientu atveseļošanos, mērot laiku, kas vajadzīgs, lai sasniegtu pilnīgu konkrētas digitālās čūlas dzīšanu katrā pacientā. Stayveer samazināja jaunu digitālo čūlu veidošanos nekā placebo. Pirmajā pētījumā pacienti, kas lietoja Stayveer, pēc 16 nedēļām vidēji saņēma 1, 4 jaunas digitālās čūlas, salīdzinot ar 2, 7 čūlas placebo ārstētiem pacientiem. Līdzīgi rezultāti tika novēroti otrajā pētījumā pēc 24 ārstēšanas nedēļām, tomēr Stayveer neietekmēja digitālo čūlu dzīšanu.
Kāds pastāv risks, lietojot Stayveer - Bosentan?
PAH gadījumā visbiežāk novērotās Stayveer blakusparādības (kas var skart vairāk nekā 1 no 10 cilvēkiem) ir galvassāpes un aknu darbības traucējumi. Pacientiem ar digitālu čūlu visbiežāk novērotās Stayveer blakusparādības (kas var skart vairāk nekā 1 no 10 cilvēkiem) ir patoloģiskas aknu darbības pārbaudes, tūska un šķidruma aizture. Ņemot vērā risku saslimt ar aknu darbības traucējumiem, ārsts noteiks aknu enzīmu līmeni pirms ārstēšanas un katru mēnesi Stayveer terapijas laikā. Pilns visu Stayveer izraisīto blakusparādību apraksts ir atrodams zāļu lietošanas pamācībā. Stayveer nedrīkst lietot pacienti, kuriem ir aknu darbības traucējumi, grūtnieces vai reproduktīvā vecuma sievietes, kas neizmanto drošas kontracepcijas metodes vai pacientus, kas ārstēti ar ciklosporīnu A (zāles, kas iedarbojas uz imūnsistēmu). Pilnīgu ierobežojumu sarakstu skatīt lietošanas instrukcijā.
Kāpēc Stayveer - Bosentan tika apstiprināts?
Aģentūras Cilvēkiem paredzēto zāļu komiteja (CHMP) nolēma, ka pacienta ieguvums, lietojot Stayveer, pārsniedz šo zāļu radīto risku, un ieteica to apstiprināt lietošanai ES.
Kādi pasākumi tiek veikti, lai nodrošinātu drošu un efektīvu Stayveer - Bosentan lietošanu?
Ir izstrādāts riska pārvaldības plāns, lai nodrošinātu, ka Stayveer tiek izmantots pēc iespējas drošāk. Pamatojoties uz šo plānu, drošuma informācija ir iekļauta Stayveer zāļu aprakstā un lietošanas instrukcijā, tostarp atbilstošie piesardzības pasākumi, kas jāievēro veselības aprūpes speciālistiem un pacientiem. Turklāt uzņēmums, kas ražo Stayveer, nodrošinās zāļu komplektu zāļu parakstītājiem un informācijas brošūru pacientiem katrā dalībvalstī, lai izskaidrotu Stayveer drošību (īpaši ņemot vērā tā ietekmi uz aknām un grūtniecības laikā) un viņa mijiedarbība. Uzņēmums arī apņemas rūpīgi uzraudzīt zāļu izplatīšanu katrā dalībvalstī un apkopot informāciju par tās lietošanu pacientiem ar progresējošu sistēmisku sklerozi ar pašreizējām digitālajām čūlām.
Vairāk informācijas par Stayveer - Bosentan
2013. gada 24. jūnijā Eiropas Komisija piešķīra Stayveer reģistrācijas apliecību, kas derīga visā Eiropas Savienībā. Plašāka informācija par ārstēšanu ar Stayveer pieejama zāļu lietošanas pamācībā (kas arī ir daļa no EPAR) vai sazinieties ar ārstu vai farmaceitu. Pēdējais šīs kopsavilkuma atjauninājums: 06-2013.